孤兒藥(Orphan drug)一般是指用於治療罕見疾病的藥物。世界衛生組織(WHO)將罕見疾病建議為罹病率低於0.65~1‰之間的疾病(註1),台灣對罕見疾病的認定則為疾病盛行率萬分之一以下為參考基準外,需經罕見疾病及藥物審議會之審查(註2)。目前全球已確認的罕見疾病約有5,000~8,000種,其中有80%的罕見疾病為遺傳缺陷所導致(註3),約有50%的罕見疾病在出生時或兒童時期即發病,而僅有約1%的罕見疾病能夠有效治療(註4),可以顯示出罕見疾病存在高度未被滿足醫療需求(unmet medical need),然受限於市場規模,長期以來並未受到製藥業所關注。
各國政府為鼓勵製藥業投入罕見疾病的新藥開發,紛紛立法增加誘因,以美國為例,在1983年立法通過孤兒藥法案(Orphan Drug Act),規定在美國境內目標治療疾病罹病人數少於20萬人,即有機會獲得孤兒藥資格認定,其他國家規定如日本為少於5萬人、歐盟為少於25萬人(註5)。如果獲醫藥主管機關認定孤兒藥資格,則可獲得一系列的優惠措施,如美國給予孤兒藥開發的優惠措施包括研發租稅優惠、市場獨佔權及政府研發補助等誘因吸引藥廠投入開發,其中最重要的市場獨佔權,不論藥品專利過期與否,該法案保障該孤兒藥自核准上市起7年的市場獨家銷售權利,歐盟與日本則皆為10年。美國在孤兒藥法案通過前僅10種藥物用在罕見疾病的治療(註6),然法案通過後累積至2013年已有超過2,900件被認定為孤兒藥(註7),超過420款藥物,可以看出法案對產業影響的成效。觀察近年來孤兒藥的認定數量,2013年美國為260件、歐盟為124件、日本為30件,2012年美國為188件、歐盟為147件、日本為32件(註8),其數量將近為2002年的三倍或以上(註9),顯示出孤兒藥逐漸為國際製藥公司所關注。
在台灣,已在2000年通過「罕見疾病防治及藥物法」及相關細則如「罕見疾病藥物供應製造及研究發展獎勵辦法」,其訂定之優惠措施如該藥品適應症之盛行率低於萬分之一則有機會獲得孤兒藥資格,並給予該孤兒藥品10年的市場獨佔期。
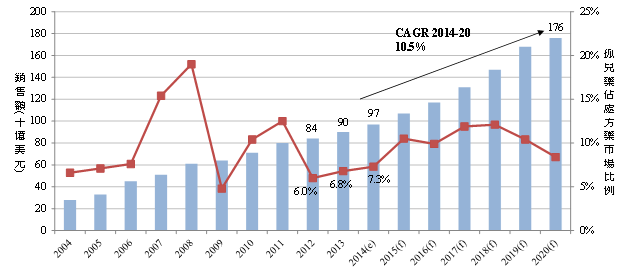
從圖1全球孤兒藥市場規模可知,在2013年全球孤兒藥銷售額約為900億美元,佔全球處方藥銷售市場13.8%,2014年約為970億美元,佔全球處方藥銷售市場14.3%,相較於整體處方藥市場,孤兒藥市場成長更為快速,預計孤兒藥市場規模與市場佔比將持續上升,至2020年市場規模將高達1,760億美元(2014-20複合年成長率10.5%),佔全球處方藥銷售市場19.1%,顯示出孤兒藥已成為藥品市場成長主要動力之一。
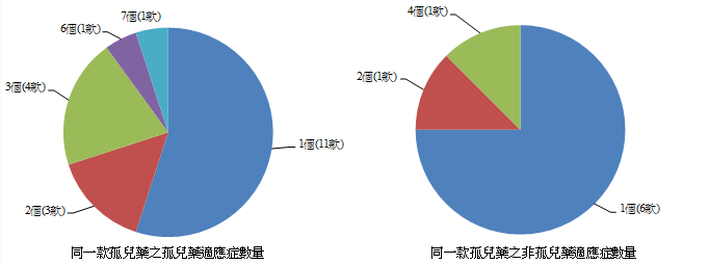
從市場面來看,孤兒藥的市場潛力較為受限,僅單一罕見疾病適應症吸引力可能不足,然而可不侷限在罕見疾病而對不同適應症持續開發,以增加市場潛力。例如Novartis的GleevecR,獲得7個孤兒藥適應症(註12)、Roche的RituxanR獲得3個孤兒藥適應症(註13)與1個非孤兒藥適應症(註14)。進一步觀察全世界前20大孤兒藥藥品的適應症數量分佈(圖2),可以發現有9款藥品(佔45%)的孤兒藥適應症在2個(含)以上,另有6款藥品更將適應症擴大至非孤兒藥適應症。
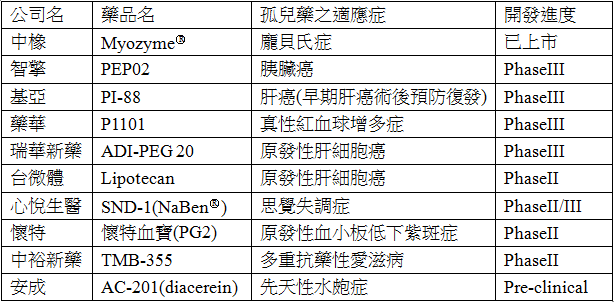
我國孤兒藥產業,除中橡所投資開發的Myozyme外,其他藥品尚處開發階段。如表1所示,計有10間廠商投入孤兒藥的開發,獲孤兒藥認定產品數佔我國新藥開發臨床階段案件之9%(註16),顯示出孤兒藥尚未成為我國新藥開發主要方向。其中治療龐貝氏症的Myozyme,由中研院陳垣崇院士在美國杜克大學投入研發,由中橡子公司Synapc進一步投資商品化開發,並與Genzyme(註17)合作,現已取得藥證上市,中橡每年可獲得美國市場銷售額的15%(註18)。智擎的PEP02用來治療胰臟癌,2003年從Hermes 公司取得授權進行開發,2011年授權給Merrimack進行歐洲及亞洲(台灣除外)的臨床開發、生產與行銷的合作,目前孤兒藥適應症胰臟癌的開發進度臨床試驗第三期已完成,預計要發表臨床最終數據與提出新藥藥證申請。基亞的PI-88的適應症為早期肝癌術後預防復發,在2000年和Progen公司策略聯盟進行開發,並於2010年取得全球使用、製造銷售之專屬授權,已完成在台灣、大陸、韓國及香港四地共25個醫學中心的第三期臨床試驗,現正蒐集臨床資料與分析。藥華的P1101在2009年授權給奧地利藥廠AOP,AOP將其適應症擴大至真性紅血球增多症而取得孤兒藥資格,歐洲的臨床試驗與歐洲、中東及前蘇聯自治共和國等地上市銷售都授權給AOP,藥華則收取里程碑金及上市後的銷售權利金(註19)。瑞華新藥隸屬於Polaris Group,其ADI-PEG20適應症為原發性肝細胞癌,已在全球進行第三期臨床試驗。其他則尚有台微體的Lipotecan、心悅生醫的SND-1、懷特的懷特血寶、中裕新藥的TMB-355與安成的AC-201,適應症分別為原發性肝細胞癌、思覺失調症、原發性血小板低下紫斑症、多重抗藥性愛滋病與先天性水皰症。
早期因罕見疾病市場有限,藥廠投入藥品開發誘因不足,直到美國孤兒藥法案通過後,製藥產業開始有了轉變。近年來更因為法規要求日益嚴格與用藥安全意識提高,使得新藥開發上市困難度上升加上常見疾病領域之治療藥物競爭逐漸激烈,進而各藥廠開始運用不同的開發策略,如因孤兒藥市場競爭者少加上各種優惠措施與獨佔的市場利益,逐漸獲得青睞。大藥廠也因面臨重磅藥(blockbuster)的專利陸續到期,而新開發藥品未能補足營收缺口下,也逐漸以中小型孤兒藥藥廠或生技公司為併購或合作標的,如2011年Sanofi-Aventis併購Genzyme。
對台灣新藥開發公司而言,在資源有限下,因法規與行政流程的優惠,孤兒藥適合成為台灣新藥開發選項之一。孤兒藥的開發,適應症的挑選成為重要的課題,除了以罕見疾病作為標的之外,如中橡Mozyme的龐貝氏症、懷特血寶的原發性血小板低下紫斑症;亦可將本來常見的疾病以亞型、病理進程、治療預後等進行標的族群切割,而取得孤兒藥資格,如基亞PI-88的早期肝癌術後預防復發、Byer的NexavarR的轉移性或無法手術切除且不適合局部治療或局部治療失敗之晚期肝細胞癌、中裕新藥的TMB-355的多重抗藥性愛滋病。此外對於台灣新藥開發公司而言,完善的適應症佈局規劃,不論是以孤兒藥進入市場進而擴大孤兒藥/非孤兒藥適應症或以非孤兒藥適應症進入市場再透過新增孤兒藥適應症增加市場獨佔銷售時間都是可以思考的方向,進而增加在國際行銷佈局、併購、策略聯盟有力的籌碼。
(註1)Rare diseases and orphan drugs- J K Aronson
(註2)申請列入罕見疾病流程-國民健康署 http://www.hpa.gov.tw/BHPNet/Web/HealthTopic/TopicBulletin.aspx?No=200804250003&parentid=200712250007
(註3)Update on 2004 Background Paper, BP 6.19 Rare Diseases-R. de Vrueh, Ph.D., E.R.F.Baekelandt, and J.M.H. de Haan http://www.who.int/medicines/areas/priority_medicines/BP6_19Rare.pdf
(註4)罕病用藥成長與市場競爭-彭嚴燕 http://cdnet.stpi.narl.org.tw/techroom/market/bio/2012/bio_12_003.htm
(註5)以盛行率作為標準,則美國為低於7.5/10,000、歐盟為5/10,000、日本為4/10,000
(註6)罕病用藥成長與市場競爭-彭嚴燕 http://cdnet.stpi.narl.org.tw/techroom/market/bio/2012/bio_12_003.htm
(註7)Orphan Drug Report 2014, EvaluatePharma
(註8)Orphan Drug Report 2014, EvaluatePharma
(註9)Orphan Drug Report 2014, EvaluatePharma;2002年孤兒藥美國認定數為64件、歐盟為52件、日本為5件
(註10)Orphan Drug Report 2014, EvaluatePharma;市場數據計算包含全球前五百大製藥與生技公司的處方藥銷售額
不包括學名藥
(註11)FDA(資料統計至2014.02.19);2011年前銷售額前二十大孤兒藥藥品Remicade、Humira、Herceptin、Rituxan、Gleevec、Revlimid、Avonex、Alimta、Velcade、Erbitux、Prograf、Tracleer、Botox、Epogen、NovoSeven、Betaseron、Kogenate、Zometa、Sandostain、Evista
(註12)7個適應症分別為Philadelphia-positive acute lymphoblastic leukemia、Gastrointestinal stromal tumors、Dermatofibrosarcoma protuberans、Chronic myelogenous leukemia、Systemic mastocytosis without the D816V c-kit mutation、Idiopathic hypereosinophilic syndrome including acute and chronic eosinophilic leukemia、Myeloproliferative disorders/Myelodysplastic syndromes associated with platelet-derived growth factor gene re-arrangements ;資料來源FDA(最後查詢日期2015.06.02)
(註13)3個孤兒藥適應症分別為Chronic lymphocytic leukemia、Non-Hodgkin’s B-cell lymphoma、Patients with anti-neutrophil cytoplasmic antibody-associated vasculitis (Wegener’s Granulomatosis, Microscopic Polyangiitis, and Churg-Strauss Syndrome);資料來源FDA (最後查詢日期為2015.06.02)
(註14)1個非孤兒藥適應症為Rheumatoid arthritis;資料來源FDA (最後查詢日期為2015.06.02)
(註15)資料統計至2015.06.02
(註16)依據2014年醫藥產業白皮書指出我國至2014.03.31日止共有國內外99件產品之新藥臨床階段的開發案;計算有扣除尚未進入臨床之AC-201
(註17)Genzyme為一間專注在孤兒藥開發之生技製藥公司,已於2011年被Sanofi-Aventis藥廠所併購
(註18)中橡孤兒藥獲15年權利金-經濟日報 http://www.finetpat.com.tw/chinese/default.asp?ID=1810
(註19)台廠孤兒藥前景法人看好-工商時報 http://www.trpma.org.tw/index.php/tw/news/item/366-台廠孤兒藥前景-法人看好
文章來源:宇智顧問股份有限公司