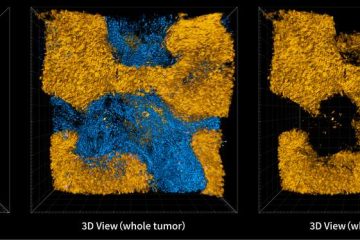
常見的癌症治療方法為外科手術、化療、放射療法與賀爾蒙療法,此外,針對特定標的之標靶藥物亦是熱門的治療方法。
各種療法有不同治療效果與限制,例如外科手術雖可切除大部分腫瘤,但卻難以處理已經發生遠端轉移的癌細胞,而現行的標靶藥物則是存在容易產生抗藥性問題。
雖然隨著治療方法的進步,癌症的存活率已明顯增加,以美國為例自1990年起癌症的死亡率每年約下降1%,預期到2015年可低於23%(註1),然因癌症的異質性(heterogeneous)與腫瘤幹細胞(cancer stem cells)等因素使得癌症一直無法全盤獲得控制,也因此在癌症治療這個領域存在著巨大的未被滿足醫療需求(unmet medical need),癌症治療一直是各藥廠兵家必爭之地。
過往熱門的標靶藥物的原理多以細胞生命週期調控機制因子(例如HER2、EGFR)與血管新生機制因子(例如VEGF)為對象;近年來從免疫調控的機制著手逐漸成為熱門的藥物開發方向,意即從促進人體的免疫力或強化免疫系統對癌細胞的辨識能力著手,使人體免疫機制針對癌細胞進行攻擊以達到治療的效果。其中發現CTLA-4(cytotoxic T-lymphocyte protein 4)與PD1(programmed cell-death protein 1)兩項分子與其功能的學者更是榮獲唐獎第一屆(2014年)生技醫藥獎(註2)。
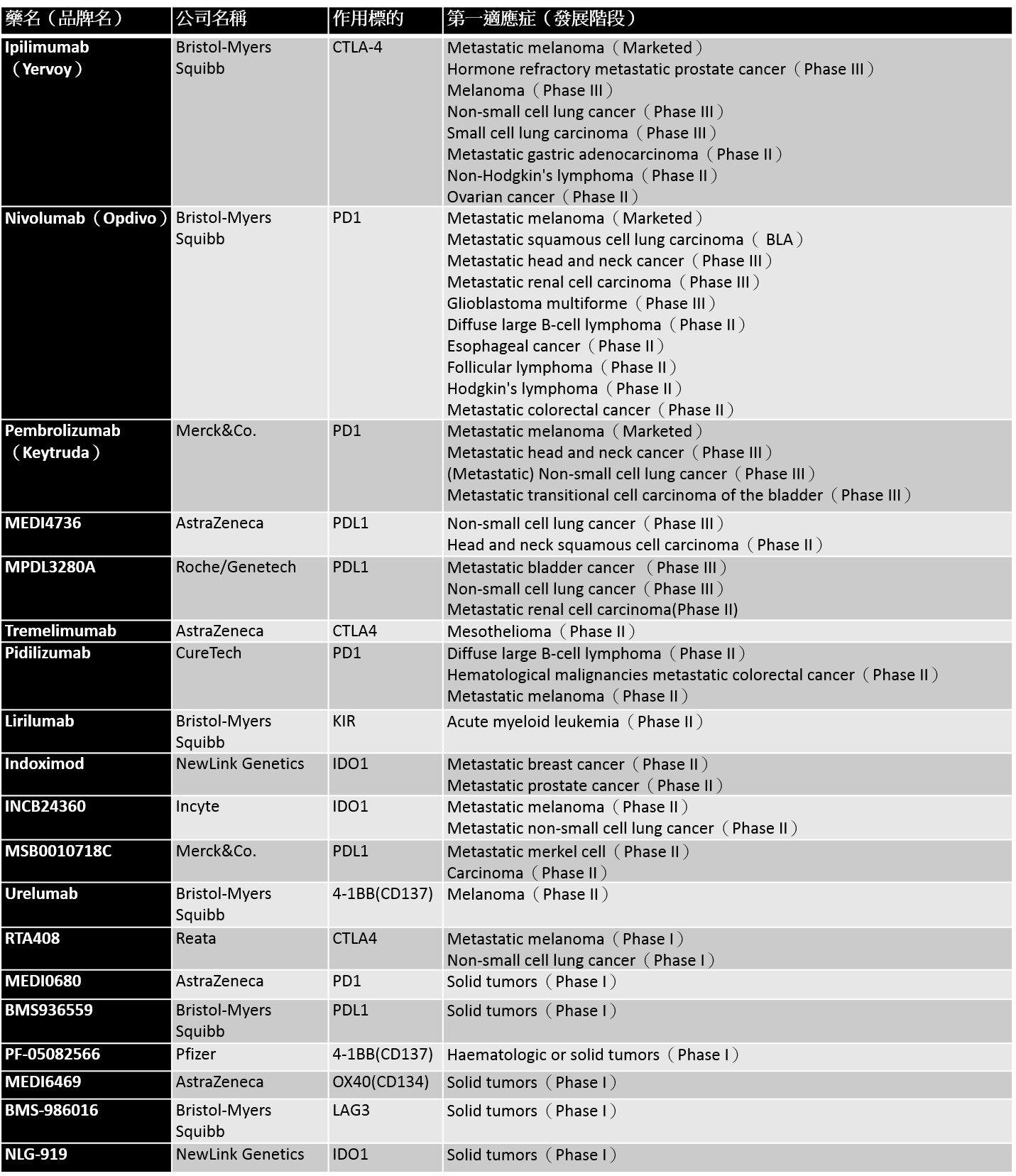
CTLA-4與PD1皆為T細胞膜上的接受器,CTLA-4可與抗原呈現細胞(antigen presenting cells)例如樹突細胞(dendrite cells)的B7分子結合以抑制T細胞的活化;而PD1則是會與癌細胞表面的PDL1結合而促使T細胞進行細胞凋亡(apoptosis)。這類接受器亦稱為免疫檢查站(checkpoint)分子,一般而言這些分子作用所產出的效應是人體為避免免疫系統失衡的機制之一,然這些機制卻亦有可能成為癌細胞藉此逃避人體免疫系統攻擊的管道(tumor immune evasion),因此,透過藥物去拮抗這些免疫checkpoint分子,會有增強免疫,進而攻擊癌細胞以達治療之效果,現已有許多臨床試驗顯示這一類藥物可有效延長許多癌症病患的存活時間與提高存活率。這類型癌症免疫療法之藥物在全球的發展現況如表1所示,其中Bristol-Myers Squibb的ipilimumab是最早上市的相關藥品,其透過拮抗CTLA-4來治療移轉性黑色素瘤(metastatic melanoma)。而Bristol-Myers Squibb的nivolumab則是最早上市用以拮抗PD-1的藥品,被核准用來治療移轉性黑色素瘤。由表1可以發現Bristol-Myers Squibb在這類藥品的發展領先全球,至少有2款藥品已上市,而有4款開發中產品已進入臨床階段,而其他藥廠如Merck&Co.、AstraZeneca、NewLink Genetics亦積極投入發展。在適應症部分可以發現黑色素瘤(Melanoma)與非小細胞肺癌(NSCLC)最備受重視。
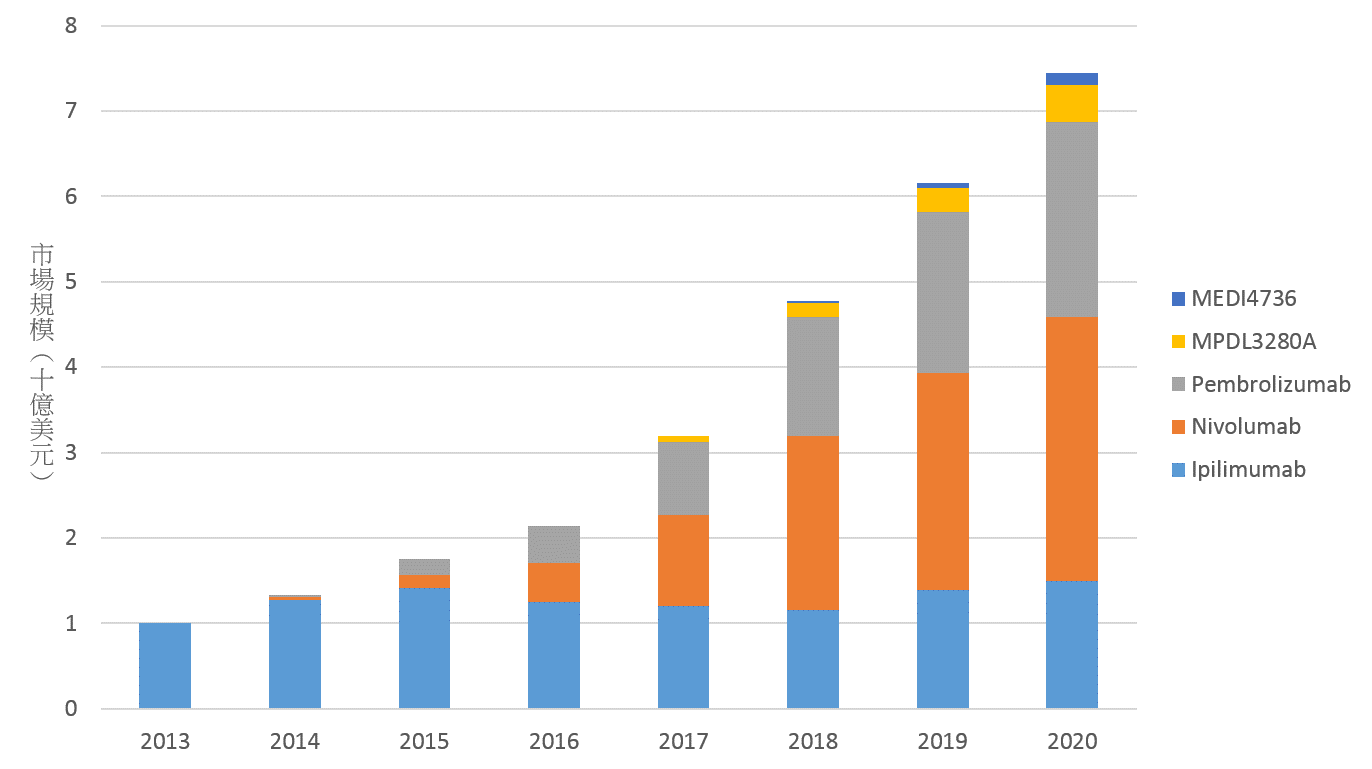
全球免疫 checkpoint抑制劑的主要市場合計如圖1所示,在2013年約10億美元,因本類藥品相對現有療法較佳的臨床表現、快速擴張的適應症與組合療法,預計以每年至少20%的成長率到2020年市場可超過70億美元,而anti-PD1藥物如nivolumab與pembrolizumab可望取得超過7成的市占率。
從臨床效果觀之,以ipilimumab為例,臨床三期試驗顯示出其單獨使用在經治療過後無法切除第三期或第四期黑色素瘤病患整體存活期(overall survival)達10.1個月,相較於僅使用gp100疫苗的6.4個月有顯著差異(P=0.003),經12個月、18個月與24個月後的存活率分別為45.6%、33.2%與23.5%(註13)。
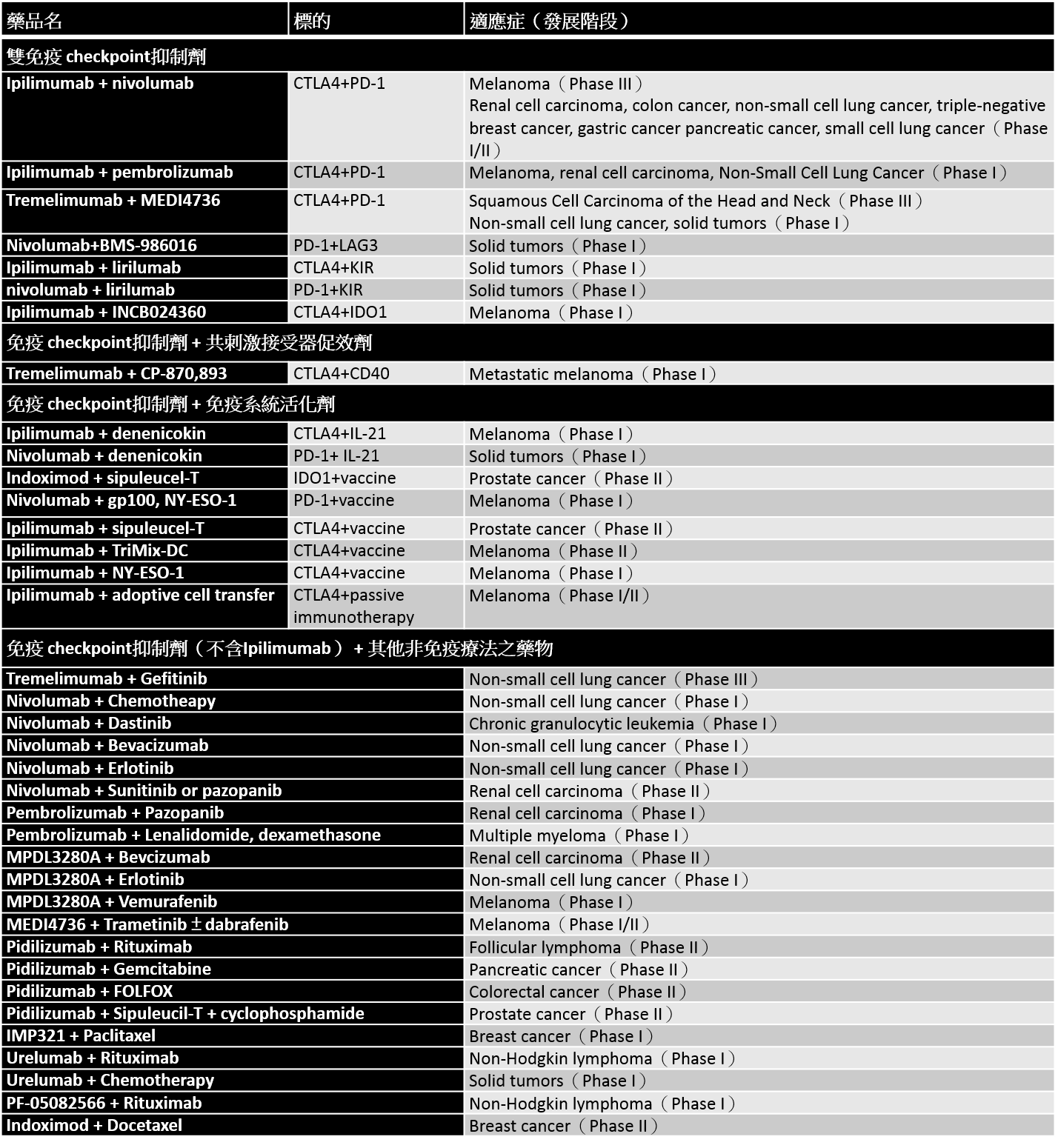
另一臨床三期試驗使用ipilimumab與dacarbazine合併治療未經治療的轉移性黑色素瘤病患整體存活期(overall survival)達11.2個月高於僅使用dacarbazine的9.1個月,而12個月、24個月與36個月存活率分別為47.3% vs 36.3%、28.5% vs 17.9%、20.8% vs 12.2%並達顯著差異(P<0.001)(註14)。從上述可知ipilimumab確實有較優異之效果,然其單獨使用反應率低,約10.9%,而使用ipilimumab與dacarbazine組合療法其反應率則提高到約為15.2%,單獨使用反應率較低可能因ipilimumab療法僅從單一免疫調控機制著手且非直接針對癌細胞,然詳細原因還有待更多研究投入,這也是許多廠商開始嘗試相關的合併療法重要原因之一(表二),如ipilimumab與和nivolumab的組合療法用於無法切除第三期或第四期黑色素瘤的反應率可提升至40%(註15)。此外AstraZeneca的MEDI4736與tremelimumab亦於2014年底前啟動合併治療鱗狀上皮細胞頭頸癌(SCCHN)的第二期試驗。
免疫 checkpoint抑制劑合併療法的開發並不僅限於免疫療法間,亦包含和其他不同治療機轉或藥物類型,例如nivolumab與gemcitabine/cisplatin治療非小細胞肺癌(NSCLC)等。
免疫checkpoint分子抑制劑不僅為癌症治療開啟了新的里程碑,亦使得過去發展緩慢的癌症免疫療法成為癌症治療的新興顯學,然而從臨床數據可以發現,雖然免疫checkpoint分子抑制劑的產生對癌症療效已有顯著的進展,然距離癌症能夠全面治癒或長期控制仍有相當距離,這使得透過多重機制去治療的組合療法已成為重要的發展方向。而台灣在相關藥物的開發上,則似乎未趕上這一波熱潮,雖然人體免疫機制複雜,但尚有機會從相關具潛力標的著手;而適應症的選擇上,考量未來臨床試驗的成本,如收案數與對照組藥品費用,從罕見癌症疾病或將特定癌症以亞型、病理進程或治療預後作切割則可為思考的方向。
(註1)A midpoint assessment of the American Cancer Society challenge goal to halve the U.S. cancer mortality rates between the years 1990 and 2015, Tim et al.
(註2)唐獎第一屆生技醫藥獎http://www.tang-prize.org/Publish.aspx?CNID=236 (最後瀏覽日期2014/12/18
(註3)The immune checkpoint inhibitors- where are we now, Rachel
(註4)Bristol-Myers Squibb http://www.bms.com/pages/default.aspx (最後瀏覽日期2014/12/18)
(註5)Merck&Co http://www.merck.com/index.html (最後瀏覽日期2014/12/18)
(註6)Reata pharmaceuticals pipeline- immune-oncology http://www.reatapharma.com/pipeline/immuno-oncology.aspx (最後瀏覽日期2014/12/18)
(註7)INCYTE Pipeline http://www.incyte.com/research/pipeline (最後瀏覽日期2014/12/18)
(註8)Merck Serono Initiates Phase II Study of Anti-PD-L1 Antibody MSB0010718C in Metastatic Merkel Cell Carcinoma http://www.fiercebiotech.com/press-releases/merck-serono-initiates-phase-ii-study-anti-pd-l1-antibody-msb0010718c-metas (最後瀏覽日期2014/12/18)
(註9)The Role of Anti-PD-L1 Immunotherapy in Cancer http://www.onclive.com/web-exclusives/the-role-of-anti-pd-l1-immunotherapy-in-cancer/6 (最後瀏覽日期2014/12/18)
(註10)Immunotherapy of melanoma with the immune costimulatory monoclonal antibodies targeting CD137, Shi-Yan & Yizhen
(註11)CTLA4 (cytotoxic T-lymphocyte protein4), PD1 (programmed cell-death protein 1), PDL1 (programmed cell-death ligand 1), KIR(killer cell immunoglobulin-like receptor), IDO1 (indoleamine 2,3-dioxygenase 1), 4-1BB (tumor necrosis factor receptor superfamily member9), OX40 (tumor necrosis factor receptor superfamily member 4)
(註12)主要市場涵蓋範圍為美國、歐盟五國與日本
(註13)Improved Survival with Ipilimumab in Patients with Metastatic Melanoma, Hodi et al.
(註14)Ipilimumab plus dacarbazine for previously untreated metastatic melanoma, Robert et al.
(註15)Nivolumab plus ipilimumab in advanced melanoma, Jedd et al.
(註16)Immuno-oncology combinations- a review of clinical experience and future prospects, Scott et al.
文章來源:宇智顧問股份有限公司