C型肝炎藥物從2013年以來有數款以HCV基因組中非結構蛋白質為作用標的之藥物獲得FDA通過,這類藥物又稱為直接抗病毒(direct-acting antiviral, DAA)藥物,因具有優異的療效與便利的給藥方式等特性,已成為近幾年感染疾病藥物領域最備受矚目的焦點。
C型肝炎簡介
根據WHO的統計顯示,全世界有超過1億8500萬的人被C型肝炎病毒(HCV)感染,造成每年約35萬人死亡。許多HCV感染的人,因症狀不明顯,使得在感染初期未診斷出或未接受治療,進而發展成慢性C型肝炎。遭受到HCV感染初六個月有急性感染症狀者稱為急性C型肝炎,一般此階段會給予免疫調節劑-干擾素(Interferon, IFN)或長效干擾素(Pegylated Interferon, pegIFN)進行治療。遭受HCV感染後,若人體未自行清除HCV或經治療然仍未清除HCV,則肝炎會進展到慢性C型肝炎(共佔約75~85%),慢性C型肝炎如持續進展,會發展到肝纖維化與肝硬化(cirrhosis),最嚴重會發展到失償性肝硬化(decompensated cirrhosis)或肝細胞癌。

C型肝炎治療方式與藥物發展
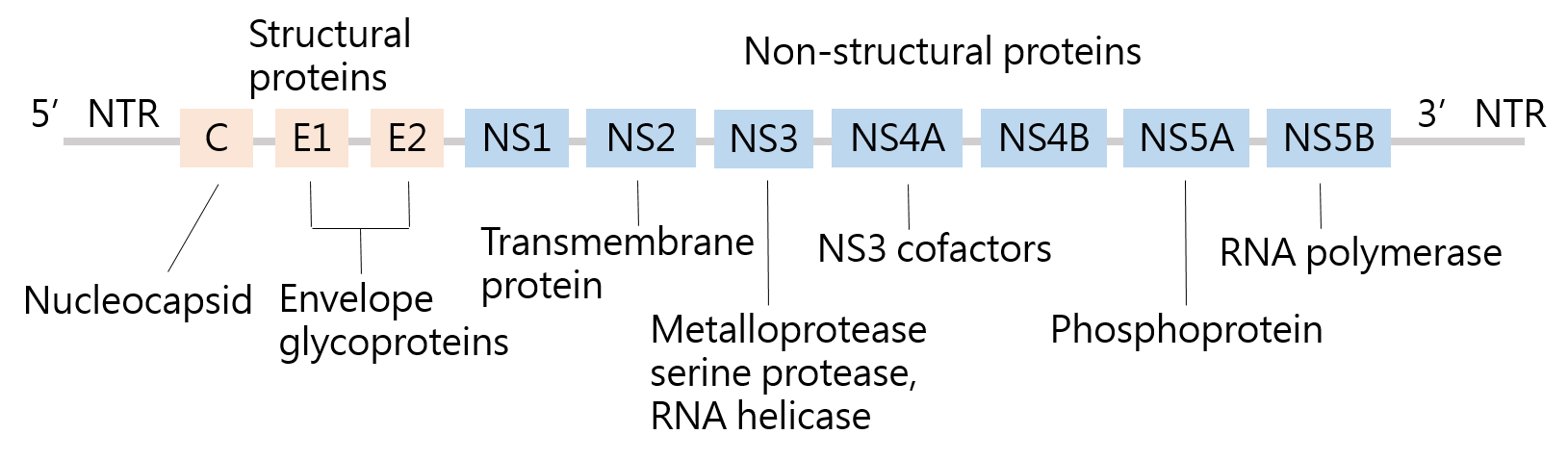
慢性C型肝炎依據不同的基因型有不同的治療成效,在過往以pegIFN加上Ribavirin為主流療法,一般以有達到持續性病毒反應(sustained viral response, SVR)為指標,pegIFN加上Ribavirin對C型肝炎治療成效有限,以人數比例最多第1基因型患者(約46.2%)為例,治癒率僅約40~50%(註1);此外使用干擾素治療具高副作用與諸多適用限制(註2,3)且療程長(達48週),使得許多病患中斷治療(註4)。在2013年因陸續上市的DAA藥物,因在C型肝炎的治療成效,使得開始出現市場相當大的轉變,該類藥物以負責C型肝炎病毒生活史之非結構性蛋白質為標的(圖2),如蛋白酶抑制劑(protease inhibitor)或RNA聚合酶抑制劑(RNA polymerase inhibitor)等,茲介紹如下:
- 首先在2013年5月屬於蛋白酶抑制劑的boceprevir(Victrelis)與telaprevir(Incivek)上市,其分別屬於Merck與Vertex公司,這類藥物成功使第1基因型C型肝炎治癒率提高到60%以上,但仍需要與pegIFN及Ribavirin合用。
- 2013年11月FDA核准Johnson&Johnson的Olysio,該藥物係為蛋白酶抑制劑,其併用pegIFN及Ribavirin可使基因型1C型肝炎治癒率約達80%(註5)。
- 2013年12月底FDA通過Gliead的sofosbuvir(Sovaldi)為C型肝炎治療帶來重大突破,其屬於RNA聚合酶抑制劑,可使大部分基因型之C型肝炎治癒率超過80%(註6),甚至在第2基因型C型肝炎治癒率可高達97%(同註6),然在第1、4基因型C型肝炎治療,Sovaldi仍需與Ribavirin及pegIFN合併使用,第2型與3型僅需與Ribavirin合併使用,在第5、6型則可能出現處方外使用(off-label use)。
- 在2014年10月Gliead再獲FDA通過一款C型肝炎劃時代藥品Harvoni,該藥品為組合藥品,包含兩個有效成份,屬於NS5A抑制劑之ledipasvir與RNA聚和酶抑制劑之sofosbuvir,為第一款獲FDA核准之免合併pegIFN之C型肝炎藥品,其對第1基因型C型肝炎治癒率可超過90%(註7)。
- 2014年底,FDA通過第二款免併用pegIFN之C型肝炎藥品,Abbvie之Viekira Pak,該款藥品亦為組合藥品,包含四個有效成份,NS5A抑制劑之ombitasvir、蛋白酶抑制劑之paritaprevir、RNA聚合酶抑制劑之dasabuvir與CYP3A抑制劑之ritonavir,其療效亦相當優秀,對於第1基因型C型肝炎治癒率也超過90%(註8)。
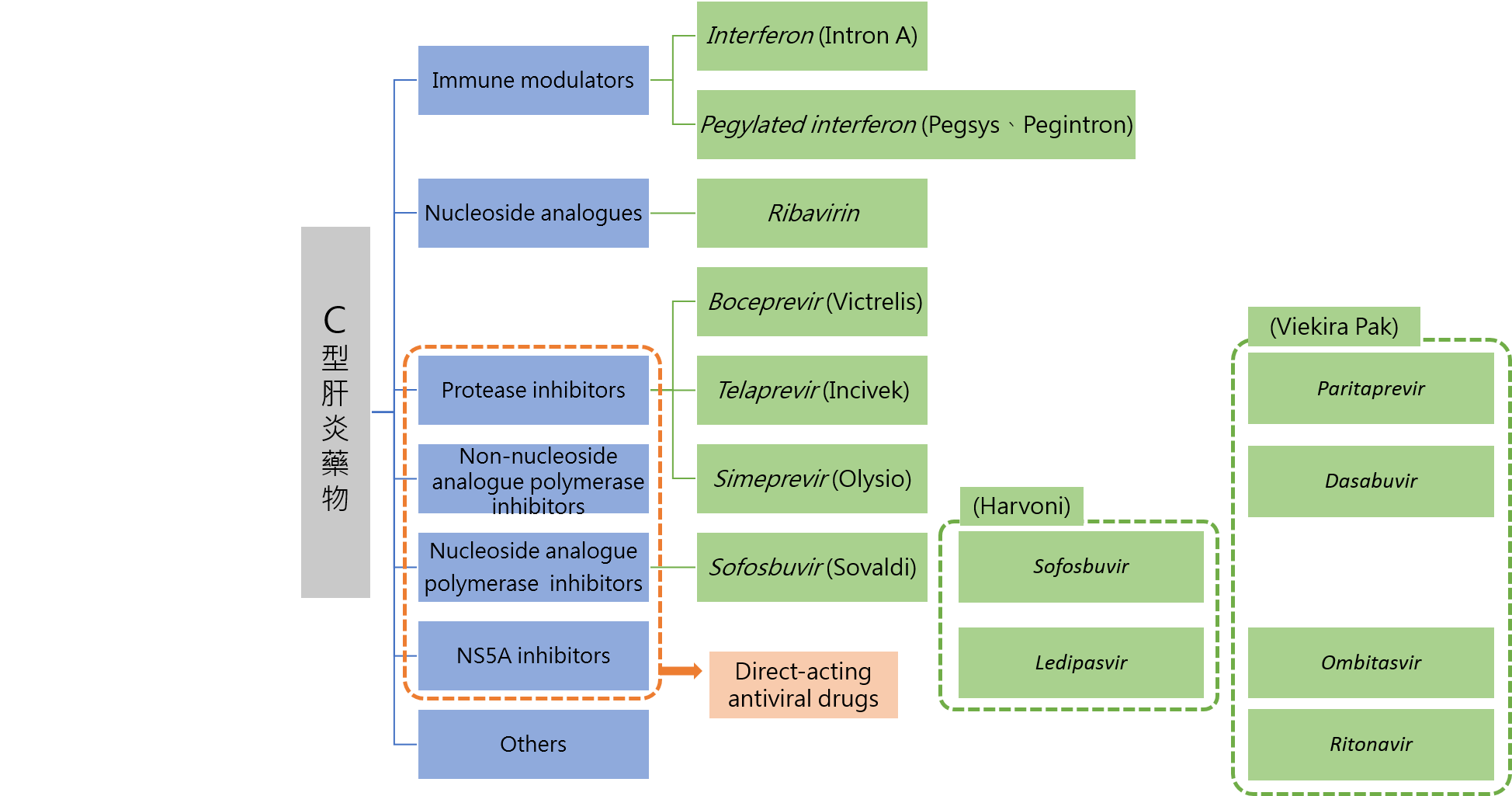
綜合上述,現今C型肝炎之治療藥品如圖3所示。
C型肝炎未被滿足的醫療需求變化
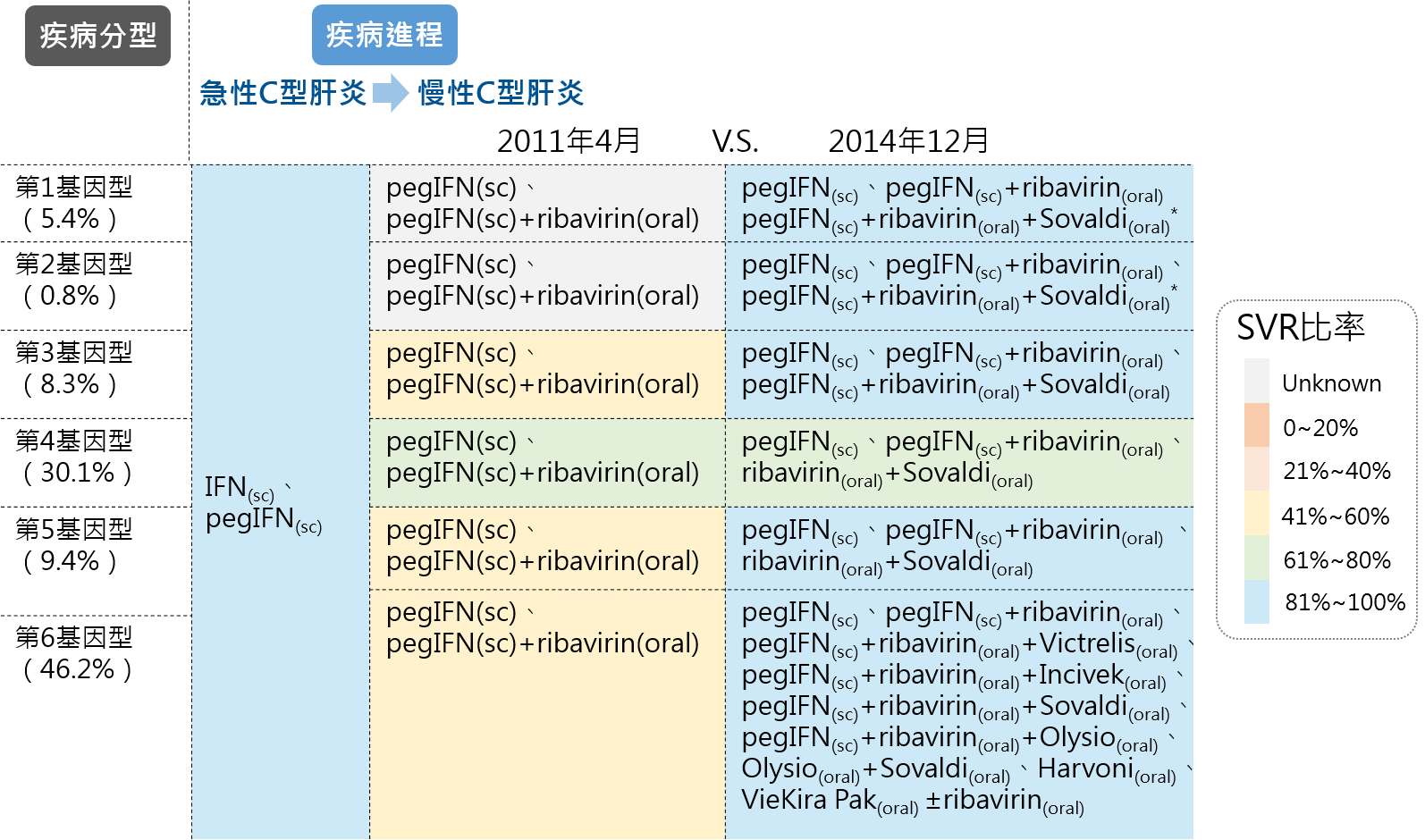
在C型肝炎之DAA藥物出來之前,從圖4可以看出C型肝炎之治療僅倚靠Ribavirin加上pegIFN為主,在治癒率部分並未有很好的成效,且pegIFN的高副作用,造成許多病患中斷治療,整體C型肝炎存在相當大的未被滿足之醫療需求(unmet medical needs)。在DAA藥物陸續上市後至2014年年底可以看出因治癒率的大幅提升,不僅使得未滿足醫療需求大幅降低,且相較於皮下注射的干擾素,口服劑型的新藥,在使用藥品上更為便利,另更將療程大幅縮短為12週或24週。
此外,圖4也顯示出可供第1基因型C型肝炎治療的藥品最多,競爭最為激烈,而在第3基因型則存在較高未被滿足的醫療需求,第5、6基因型尚倚賴於Sovaldi的處方外使用來治療,還有待藥品適應症的正式擴張。
C型肝炎藥物競爭現況
DAA藥物的出現使C型肝炎治療出現典範轉移,也就是過往的標準治療方式出現重大轉變。在這些DAA藥物中,首先上市的telaprevir與boceprevir,可降低療程時間,在上市之初被視為一大優點,而因telaprevir的療效約略優於boceprevir且其副作用的控制管理亦較容易(註15),因此telaprevir的市場表現可預期比boceprevir佳(註16)。
被視為突破性療法的藥物Sovaldi,雖仍需併用Ribavirin與pegIFN,然因優異的治療成效、泛基因型的治療廣度與昂貴價格備受關注,其銷售額在2014年快速竄升至102.8億美元,僅次於Humira(註17)。
此外最受矚目DAA藥物則是Harvoni,其以優異的療效、方便的服用方式(一天一粒口服)、免併用Ribavirin與pegIFN,其在上市後8週在隸屬於全美第二大PBM公司CVS Caremark的處方量甚至超過Sovaldi達2.5倍,可望在未來C型肝炎藥物市場中取得主導性的地位(註18)。然而Sovaldi與Harvoni因高藥價遭遇到來自市場的挑戰,例如美國最大的PBM公司Express Scripts將之排除在第1基因型C型肝炎藥品給付目錄之外(註19,20),預期使Sovaldi與Harvoni的市場遭受VieKira Pak的挑戰。
VieKira Pak雖為口服藥品且療效與Harvoni差異不大,然其服用方式相較於Harvoni稍加不便(每天早上服用ombitasvir、paritaprevir、ritonavir與dasabuvir,每晚服用dasabuvir(註21)),以及可能需併用ribavirin(註22),使其競爭力低於Harvoni,而其採價格面競爭的策略,獲得Express Scripts的支持,會有助於增加其銷售額與市佔率的成長。
Olysio屬於第二代的蛋白酶抑制劑,雖相較於telaprevir與boceprevir已經有更低的HCV抗藥性機率與更方便的服用時程(一天一粒)(註23),然仍需併用Ribavirin與pegIFN,且甫上市之初即面對Sovaldi的強勢競爭,處於不利的局面,雖然後來發展出與Sovaldi併用的治療方式,可免除併用pegIFN與ribavirin,然此治療方式進一步遭受後來上市Harvoni的競爭,使其銷售額持續萎縮(註24)。綜合上述,各藥物的競爭力形塑其市場表現,整體市佔率的變化如圖5所示。
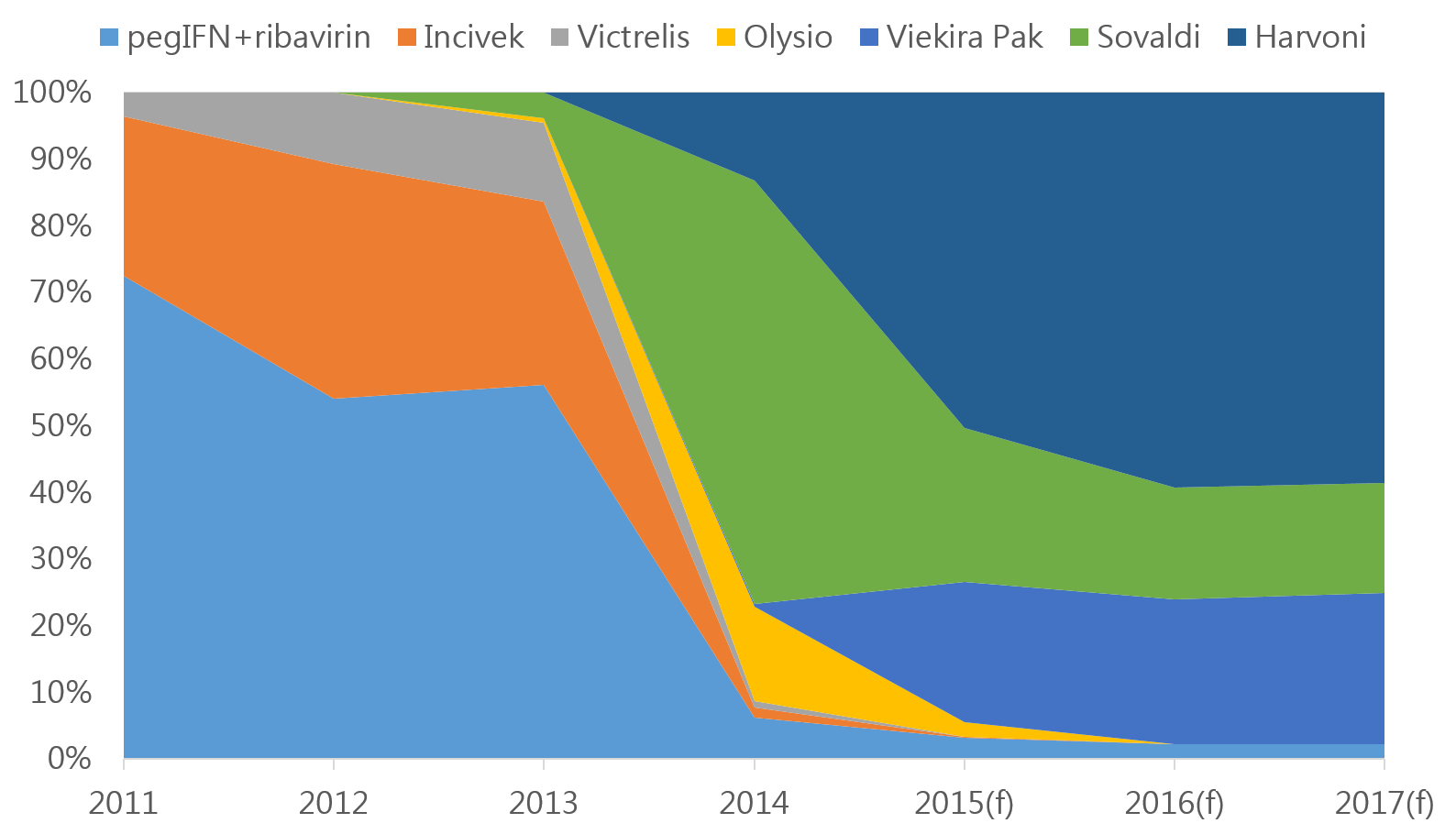
C型肝炎藥物市場未來展望
C型肝炎過往因干擾素的副作用,使得許多人中斷C肝的治療,而這為數眾多的病患被稱為warehoused patients;此外C型肝炎是進程緩慢的疾病,被診斷出HCV感染後未必有需要接受立即性的治療,然而免合併干擾素口服藥物的出現與療效上重大的突破,促使這些病患出來接受藥物治療,這會是C肝藥物市場成長的重要動力之一;再加上較昂貴的藥價,可能會促使整體HCV治療的市場規模提高2~3倍;此外雖然第1基因型C型肝炎的病患佔比最高,然可供該基因型之藥物間的競爭亦已進入白熱化階段,預期該市場的成長會稍緩;而Gliead的藥物Sovaldi在第2與第3基因型C肝病患的治療與Harvoni在第2與3基因型標示外使用會是市場進一步成長的驅動力之一。整體而言,預期全球C型肝炎藥物市場會從2012年的約47億美元成長數倍到2017年約177億美元(註25,26)。
在藥品競爭方面,Gilead的Harvoni因其優異的臨床效果、低副作用與口服劑型的特性,有機會成為第1基因型C型肝炎的黃金治療準則,此外再加上其first-to-market(註27)的優勢,有助於成為第一線用藥偏好的選擇,後續同類型藥物的競爭者主要會是在價格方面給予競爭壓力。而Ribavirin加上免疫調節劑-長效干擾素(pegIFN),為DAA藥物現世前的主流治療方法,基於DAA藥物藥價與全球各國法規主關機關陸續核准與產品鋪貨時程,現在仍然是重要的治療方式之一,但預期會治療對象會逐漸限縮至僅對DAA藥物無效者、病患需服用的藥物會和DAA藥物有嚴重交互作用者與經濟水準較低的地區(註28)。然值得注意的是,Gilead對第三世界市場的authorized generic program授權的模式(註29,30),不僅有助於Gilead的HCV藥品在第三世界市場的版圖擴張,亦會加快壓低干擾素在這些地區HCV藥品市場的市佔率。
2013年之後的幾年間見證了C型肝炎治療發生典範轉移,全新的藥品類型與作用機制帶給人類在C型肝炎治療顯著的進步,同時上一代的治療方式亦將逐步被汰除。在C型肝炎藥品間市場表現的消長,可以看出藥品的競爭力受到療效、安全性、施用方式與療程所影響,而Harvoni與VieKira Pak的出現更宣示著C型肝炎的藥物進入了組合療法的時代。在C型肝炎未滿足醫療需求逐漸縮小且市場競爭越趨激烈時,相對的市場潛力亦被限縮,後續C型肝炎新藥品發展的方向與策略是值得後進者審慎考量的。
(註1)C型肝炎病毒基因分型及其臨床重要性,謝佩真等
(註2)干擾素副作用包含有神經精神事件(neuropsychiatric events),類感冒症狀(flu-like symptoms)與血液毒性(haematological toxicities)。
(註3)Novel therapies for hepatitis C- on pill fits all?, Michael P. & Thomas von
(註4)All oral HCV therapies near approval, Man Tsuey Tse
(註5)Simeprevir with pegylated interferon alfa 2a plus ribavirin in treatment-naive patients with chronic hepatitis C virus genotype 1 infection (QUEST-1): a phase 3, randomised, double-blind, placebo-controlled trial, Jacobson et al.(註6)Sofosbuvir for previously untreated chronic hepatitis C infection, Lawitz et al.
(註7)Ledipasvir and sofosbuvir for untreated HCV genotype 1 infection, Afdhal et al.
(註8)Treatment of HCV with ABT-450/r-ombitasvir and dasabuvir with ribavirin, Feld et al.
(註9)Hepatitis C therapeutics: current status and emerging strategies, Tan et al
(註10)Hepatitis C Virus: Molecular Pathways and Treatment, Oumaima
(註11)資料來源:急性C型肝炎治療之建議,黃信彰
(註12)The clinical importance of hepatitis C genotyping in the United States, Scott
(註13)Ledipasvir and sofosbuvir for 8 or 12 weeks for chronic HCV without cirrhosis, Kowdley et al
(註14)Global distribution and prevalence of hepatitis C virus genotypes, Jane et al
(註15)Telaprevir的副作用主要為皮疹(skin rash),可用類固醇控制。Boceprevir的副作用主要為貧血,可用紅血球生成刺激劑(erythropoiessi-stimulaing agent, ESA),除了價格較類固醇昂貴外,在歐洲可能會受限於RBV相關缺血HCV患者尚未被核准使用ESA藥物。
(註16)Hepatitis C- pipeline update, Irena Melnikova
(註17)The best selling prescription drugs in the world last year http://qz.com/349929/best-selling-drugs-in-the-world/(最後瀏覽時間2015/03/16)
(註18)Harvoni utilization in the weeks after lunch: patterns and implications, Alan et al
(註19)AbbVie Deal Heralds Changed Landscape for Hepatitis Drugs, Andrew Pollack
(註20)Express Scripts gives AbbVie exclusive Hepatitis C billing, Meg Tirrell
(註21)VieKira Pak仿單
(註22)第1a基因型、第1b基因型且有肝硬化者需併用ribavirin
(註23)Novel therapies for hepatitis C- one pill fits all, Michael P. & Thomas von
(註24)Johnson & Johnson looks to “remain competitive” in hepatitis C market, Joe Barber http://www.firstwordpharma.com/node/1240093#axzz3Gc4OImuC (最後瀏覽日期2015/03/16)
(註25)Consensus outlook- hepatitis C-game-changing regimens to revolutionise treatment landscape, Firstword
(註26)C型肝炎藥物市場發生跳躍式的成長從歷史來看有脈絡可循,當Merck的PEG-Intron於2001年上市後,在美國尋求治療的患者增加了3倍,全球市場則進一步從2001年的14.5億美元成長到2003年的29億美元,近2倍。(資料來源:同註19)
(註27)從interferon-free與ribavirin-free的觀點來看
(註28)Novel therapies for hepatitis C- one pill fits all, Michael P. & Thomas von
(註29)$10 Copy of Gilead Blockbuster Sovaldi Appears in Bangladesh http://www.bloomberg.com/news/articles/2015-03-08/-10-copy-of-gilead-s-blockbuster-sovaldi-appears-in-bangladesh
(註30)Gilead Sciences, Inc.: Access Program, V. Kasturi Rangan & Katharine Lee
文章來源:宇智顧問股份有限公司